Назовите основные типы химической связи

Основными типами химической связи являются:
- Ковалентная связь: Ковалентная связь образуется, когда два или более атомов делятся электронами. Это приводит к образованию прочной связи между атомами, причем каждый атом вносит равный вклад в общую пару электронов. Ковалентные связи обычно образуются между атомами неметаллов.
- Ионная связь: Ионные связи образуются между положительно заряженными ионами (катионами) и отрицательно заряженными ионами (анионами). Связь образуется в результате электростатического притяжения между ионами, которое возникает в результате переноса электронов от одного атома к другому. Ионные связи обычно образуются между металлическими и неметаллическими атомами.
- Металлическая связь: Металлическая связь возникает в металлах и является результатом обмена электронами между атомами металла. Электроны могут свободно перемещаться по решетке металла, что приводит к характерной электрической и тепловой проводимости металлов.
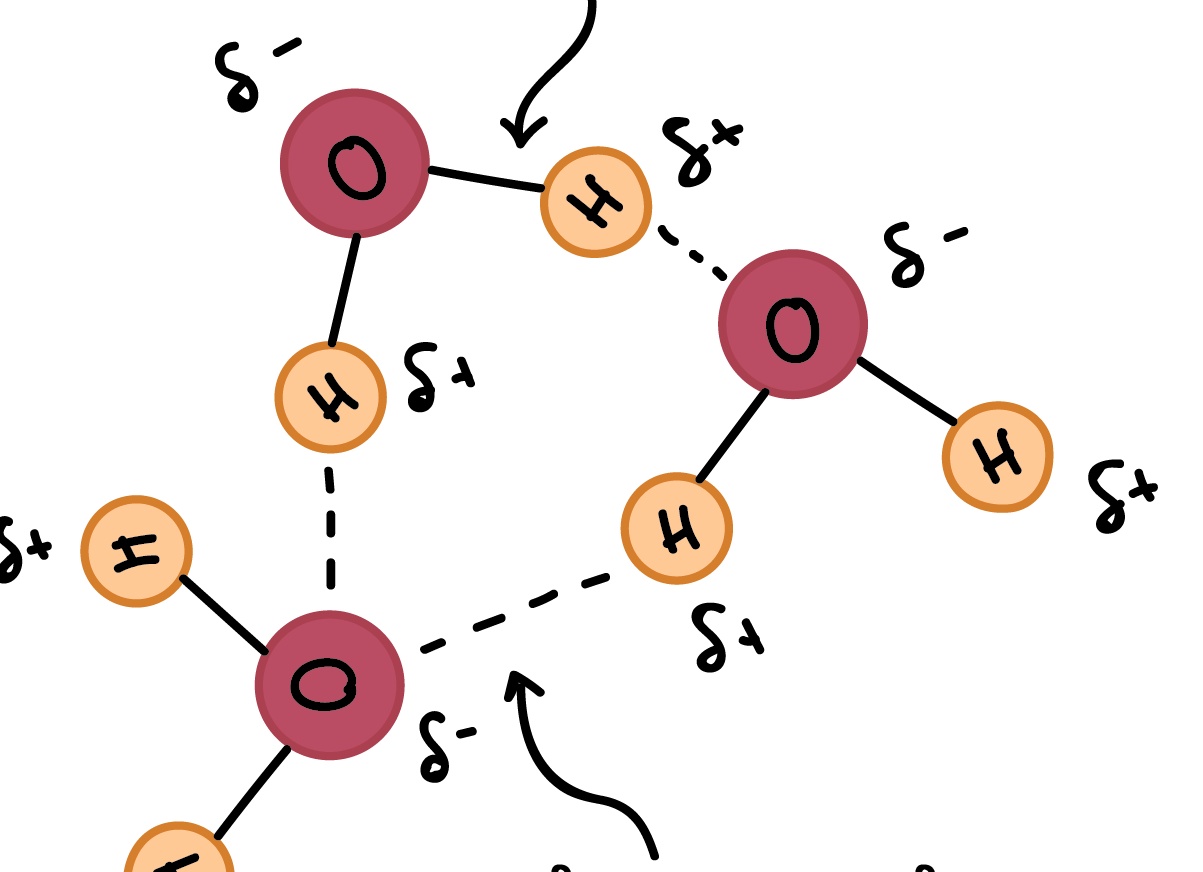
- Водородная связь: Водородная связь — это тип слабой связи, которая образуется между атомами водорода, ковалентно связанными с высокоэлектронегативными атомами, такими как азот, кислород или фтор. Водородные связи играют важную роль в определении свойств и поведения многих веществ, включая воду.
Эти типы связей не являются взаимоисключающими, и молекула может содержать несколько типов связей. Тип и прочность связи определяют многие физические и химические свойства молекулы, такие как стабильность, реакционная способность и растворимость.









Комментарии 0